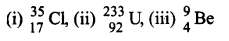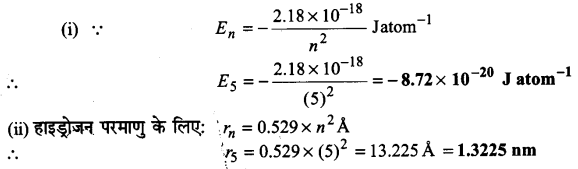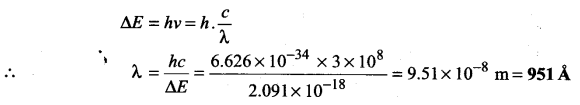NCERT Solutions Class 11 रसायन विज्ञान Chapter-2 (परमाणु की संरचना)
Class 11 (रसायन विज्ञान )
अभ्यास के अन्तर्गत दिए गए प्रश्नोत्तर
पाठ-2 (परमाणु की संरचना)
अभ्यास के अ न्तर्गत दिए गए प्रश्नोत्तर
प्रश्न 1.
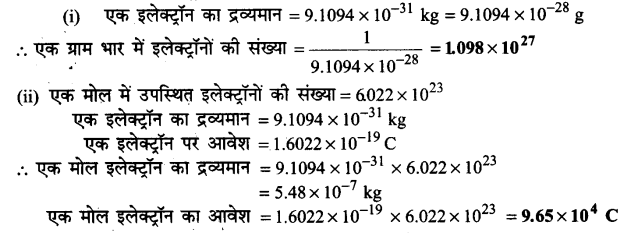
(i) एक ग्राम भार में इलेक्ट्रॉनों की संख्या का परिकलन कीजिए।
(ii) एक मोल इलेक्ट्रॉनों के द्रव्यमान और आवेश का परिकलन कीजिए।
उत्तर :
प्रश्न 2.
(i) मेथेन के एक मोल में उपस्थित इलेक्ट्रॉनों की संख्या का परिकलन कीजिए।
(ii) 7mg14C में न्यूट्रॉनों की
(क) कुल संख्या तथा
(ख) कुल द्रव्यमान ज्ञात कीजिए। (न्यूट्रॉन का द्रव्यमान =1.675×10-27 kg मान लीजिए।)
(iii) मानक ताप और दाब(STP) पर 34 mg NH3 में प्रोटॉनों की
(क) कुल संख्या और
(ख) कुल द्रव्यमान बताइए।
दाब और ताप में परिवर्तन से क्या उत्तर परिवर्तित हो जाएगा?
उत्तर :
प्रश्न 3.
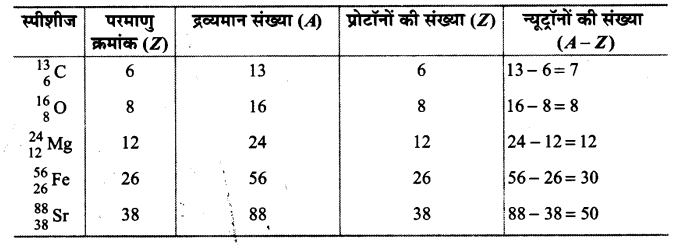
निम्नलिखित नाभिकों में उपस्थित न्यूट्रॉनों और प्रोटॉनों की संख्या बताइए-
उत्तर :
प्रश्न 4.
नीचे दिए गए परमाणु द्रव्यमान (A) और परमाणु संख्या (Z) वाले परमाणुओं का पूर्ण प्रतीक लिखिए-
(i) Z = 1,A = 35
(ii) Z = 92, A = 233
(iii) Z = 4, A = 9
उत्तर :
प्रश्न 5.
सोडियम लैम्प द्वारा उत्सर्जित पीले प्रकाश की तरंगदैर्घ्य (λ) 580 mm है। इसकी आवृत्ति (v) और तरंग-संख्या (V) की परिकलन कीजिए।
उत्तर :
प्रश्न 6.
प्रत्येक ऐसे फोटॉन की ऊर्जा ज्ञात कीजिए-
(i) जो 3×1016 Hz आवृत्ति वाले प्रकाश के संगत हो।
(ii) जिसकी तरंगदैर्घ्य 0:50 A हो।
उत्तर :
प्रश्न 7.
2.0×10-10 s काल वाली प्रकाश तरंग की तरंगदैर्घ्य, आवृत्ति और तरंग-संख्या की गणना कीजिए।
उत्तर :
प्रश्न 8.
ऐसा प्रकाश, जिसकी तरंगदैर्घ्य 4000 pm हो और जो 1J ऊर्जा दे, के फोटॉनों की संख्या बताइए।
उत्तर :
प्रश्न 9.
यदि 4×10-7m तरंगदैर्घ्य वाला एक फोटॉन 2.13 ev कार्यफलन वाली धातु की सतह स’ टकराता है तो-
(i) फोटॉन की ऊर्जा (ev में)
(ii) उत्सर्जन की गतिज ऊर्जा और
(iii) प्रकाशीय इलेक्ट्रॉन के वेग का परिकलन कीजिए। (1 eV = 1,6020 x 10-19 J)
उत्तर :
प्रश्न 10.
सोडियम परमाणु के आयनंन के लिए 242 nm तरंगदैर्ध्य की विद्युत-चुम्बकीय विकिरण पर्याप्त होती है। सोडियम की आयनन ऊर्जा kJ mol-1 में ज्ञात कीजिए।
उत्तर :
प्रश्न 11.
25 वाट का एक बल्ब 0.57um तरंगदैर्घ्य वाले पीले रंग का एकवर्णी प्रकाश उत्पन्न करता है। प्रति सेकण्ड क्वाण्टा के उत्सर्जन की दर ज्ञात कीजिए।
उत्तर :
प्रश्न 12.
किसी धातु की सतह पर 6800 A तरंगदैर्ध्व वाली विकिरण डालने से शून्य वेग वाले इलेक्ट्रॉन उत्सर्जित होते हैं। धातु की देहली आवृत्ति (v°) और कार्यफलन (W°) ज्ञात
कीजिए।
उत्तर :
प्रश्न 13.
जब हाइड्रोजन परमाणु के n= 4ऊर्जा स्तर से n= 2 ऊर्जा स्तर में इलेक्ट्रॉन जाता है तो किस तरंगदैर्घ्य का प्रकाश उत्सर्जित होगा?
उत्तर :
प्रश्न 14.
यदि इलेक्ट्रॉन n=5 कक्षक में उपस्थित हो तो H-परमाणु के आयनन के लिए कितनी ऊर्जा की आवश्यकता होगी? अपने उत्तर की तुलना हाइड्रोजन परमाणु के आयनन एन्थैल्पी से कीजिए। (आयनन एन्थैल्पी n=1 कक्षक से इलेक्ट्रॉन को निकालने के लिए आवश्यक ऊर्जा होती है।)
उत्तर :
प्रश्न 15.
जब हाइड्रोजन परमाणु में उत्तेजित इलेक्ट्रॉन = 6 से मूल अवस्था में जाता है तो प्राप्त उत्सर्जित रेखाओं की अधिकतम संख्या क्या होगी?
उत्तर :
उत्सर्जित रेखाओं की प्राप्त संख्या 15 होगी। यह निम्न संक्रमणों के कारण प्राप्त होंगी-
प्रश्न 16.
(i) हाइड्रोजन के प्रथम कक्षक से सम्बन्धित ऊर्जा – 2.18×10-18Jatom-1 है पाँचवें कक्षक से सम्बन्धित ऊर्जा बताइए।
(ii) हाइड्रोजन परमाणु के पाँचवें बोर कक्षक की त्रिज्या की गणना कीजिए।
उत्तर :
प्रश्न 17.
हाइड्रोजन परमाणु की ‘बामर श्रेणी में अधिकतम तरंगदैर्घ्य वाले संक्रमण की तरंग-संख्या की गणना कीजिए।
उत्तर :
बामर श्रेणी में अधिकतम तरंगदैर्घ्य वाले संक्रमण के लिए
प्रश्न 18.
हाइड्रोजन परमाणु में इलेक्ट्रॉन को पहली कक्ष से पाँचवीं कक्ष तक ले जाने के लिए आवश्यक ऊर्जा की जूल में गणना कीजिए। जब यह इलेक्ट्रॉन तलस्थ अवस्था में लौटता है तो किस तरंगदैर्घ्य का प्रकाश उत्सर्जित होगा? (इलेक्ट्रॉन की तलस्थ अवस्था ऊर्जा -2.18 x 10-11erg है)।
उत्तर :
प्रश्न 19.
हाइड्रोजन परमाणु में इलेक्ट्रॉन की ऊर्जा En = द्वारा दी जाती है। n=2 कक्षा से इलेक्ट्रॉन को पूरी तरह निकालने के लिए आवश्यक ऊर्जा की गणना कीजिए। प्रकाश की सबसे लम्बी तरंगदैर्घ्य (cm में) क्या होगी जिसका प्रयोग इस | संक्रमण में किया जा सके?
उत्तर :
प्रश्न 20.
2.05 x 107ms-1 वेगं से गंति कर रहे किसी इलेक्ट्रॉन का तरंगदैर्ध्य क्या होगी?
उत्तर :
दे-ब्रॉग्ली समीकरण के अनुसार,
प्रश्न 21.
इलेक्ट्रॉन का द्रव्यमान 9.1×10-31kg है। यदि इसकी गतिज ऊर्जा 3.0×10-25 Jहो तो इसकी तरंगदैर्घ्य की गणना कीजिए।
उत्तर :
प्रश्न 22.
निम्नलिखित में से कौन सम-आयनी स्पीशीज हैं, अर्थात् किनमें इलेक्ट्रॉनों की समान संख्या है?
Na+, K+, Mg2+, Ca2+, S2-,Ar
उत्तर :
दी गई स्पीशीज में इलेक्ट्रॉन्स की संख्या निम्नवत् है-
प्रश्न 23.
(i) निम्नलिखित आयनों का इलेक्ट्रॉनिक विन्यास लिखिए
(क) H–
(ख) Na+
(ग) O2-
(घ) F–
(ii) उन तत्वों की परमाणु संख्या बताइए जिनके सबसे बाहरी इलेक्ट्रॉनों को निम्नलिखित रूप में दर्शाया जाता है-
(क) 3s1
(ख) 2p3 तथा
(ग) 3p5
(iii) निम्नलिखित विन्यासों वाले परमाणुओं के नाम बताइए-
(क) [He] 2s1
(ख) [Ne] 3s23p3
(ग) [Ar]4s23d1
उत्तर :
प्रश्न 24.
किस निम्नतम n मान द्वारा g-कक्षक का अस्तित्व अनुमत होगा?
उत्तर :
g उपकोश के लिए, 1 = 4
चूँकि । का मान 0 तथा (n-1) के बीच होता है, g-कक्षक के अस्तित्व के लिए ॥ का निम्नतम मान n = 5 होगा।
प्रश्न 25.
एक इलेक्ट्रॉन किसी 3d-कक्षक में है। इसके लिए n, 1 और m1 के सम्भव मान दीजिए।
उत्तर :
3d कक्षक के लिए, n = 3,1=2
1=2 के लिए, m1=-2,-1, 0, +1, +2
इस प्रकार, दिये गये इलेक्ट्रॉन के लिए।
n= 3,1= 2, m1 = -2, -1, 0, +1,+ 2
प्रश्न 26.
किसी तत्व के परमाणु में 29 इलेक्ट्रॉन और 35 न्यूट्रॉन हैं-
(i) इसमें प्रोटॉनों की संख्या बताइए।
(ii) तत्व का इलेक्ट्रॉनिक विन्यास बताइए।
उत्तर :
एक उदासीन परमाणु के लिए
Z= प्रोटॉनों की संख्या = इलेक्ट्रॉनों की संख्या
इसलिए, दिये गये तत्त्व का परमाणु क्रमांक (Z) = 29
(i) इसमें उपस्थित प्रोटॉनों की संख्या = 29
(ii) दिये गये तत्त्व को इलेक्ट्रॉनिक विन्यास निम्न है-
1s2 2s2 2p6 3s2 3p6 3d10 4s1 or [Ar]3d10 4s1
प्रश्न 27.
, H2 और
स्पीशीज में उपस्थित इलेक्ट्रॉनों की संख्या बताइए।
उत्तर :
H2 में उपस्थित इलेक्ट्रॉनों की संख्या = 1+1=2
में उपस्थित इलेक्ट्रॉनों की संख्या = 2-1=1
में उपस्थित इलेक्ट्रॉनों की संख्या = (8+ 8)-1= 15
प्रश्न 28.
(i) किसी परमाणु कक्षक का n = 3 है। उसके लिए। और 2m1 के सम्भव मान क्या होंगे ?
(ii) 3d-कक्षक के इलेक्ट्रॉनों के लिए m1 और क्वाण्टम संख्याओं के मान बताइए।
(iii) निम्नलिखित में से कौन-से कक्षक सम्भव हैं
lp, 2s, 22 और 3f
उत्तर :
प्रश्न 29.
s, p, 4 संकेतन द्वारा निम्नलिखित क्वाण्टम संख्याओं वाले कक्षकों को बताइए–
(क) n = 1; l= 0
(ख) n = 3:l=1
(ग) n = 4;1= 2
(घ) n = 4:1= 3
उत्तर :
(क) as
(ख) 3p
(ग) 4d
(घ) 4f
प्रश्न:30.
कारण देते हुए बताइए कि निम्नलिखित क्वाण्टम संख्या के कौन-से मान सम्भव नहीं हैं-
उत्तर :
(क) सम्भव नहीं है, क्योंकि n का मान कभी शून्य नहीं होता।
(ख) सम्भव है।
(ग) सम्भव नहीं है, क्योंकि जब n=1,1= 0 केवल
(घ) सम्भव है।
(ङ) सम्भव नहीं है, क्योंकि जब n= 3,1= 0, 1, 2
(च) सम्भव है।
प्रश्न 31.
किसी परमाणु में निम्नलिखित क्वाण्टम संख्याओं वाले कितने इलेक्ट्रॉन होंगे
(क) n=4, m2 =
(ख) n= 3,l= 0
उत्तर :
प्रश्न 32.
यह दर्शाइए कि हाइड्रोजन परमाणु की बोर कक्षा की परिधि उस कक्षा में गतिमान इलेक्ट्रॉन की दे-ब्राग्ली तरंगदैर्घ्य को पूर्ण गुणक होती है।
उत्तर :
2πr बोर कक्षक की परिधि को इर्शाता है। इस प्रकार, हाइड्रोजन परमाणु के लिए बोर कक्षक की परिधि दे-ब्रॉग्ली तरंगदैर्ध्य की पूर्ण गुणांक होगी।
प्रश्न 33.
He+ स्पेक्ट्रम के += 4 से n = 2 बामर संक्रमण से प्राप्त तरंगदैर्घ्य के बराबर वाला संक्रमण हाइड्रोजन स्पेक्ट्रम में क्या होगा?
उत्तर :
हाइड्रोजन जैसी स्पीशीज़ के लिए
यह तभी सम्भव है जब n1 =1 तथा ny = 2 हो।
अत: H स्पेक्ट्रम में समान तरंगदैर्घ्य के लिए संगत संक्रमण n=2 से n=1 होगा।
प्रश्न 34.
He+ (g) → He+ (g) +e– प्रक्रिया के लिए आवश्यक ऊर्जा की गणना कीजिए।
हाइड्रोजन परमाणु की तलस्थ अवस्था में आयनन ऊर्जा 2.18 x 10-18Jatom-1 है।
उत्तर :
हाइड्रोजन जैसी स्पीशीज के लिए, nth कक्षक की ऊर्जा निम्न व्यंजक से प्राप्त की जा सकती है-
प्रश्न 35.
यदि कार्बन परमाणु का व्यास 0.15 nm है तो उन कार्बन परमाणुओं की संख्या की गणना कीजिए जिन्हें 20 cm स्केल की लम्बाई में एक-एक करके व्यवस्थित किया जा सकता है।
उत्तर :
कार्बन परमाणु का व्यास = 0.15 nm = 1.5×10-10m=1.5×10<sup-8+ cm स्केल की लम्बाई जिसमें कार्बन परमाणु व्यवस्थित हैं = 20cm
∴ कार्बन परमाणुओं की संख्या जों स्केल की लम्बाई में एक-एक करके व्यवस्थित होंगे-
प्रश्न 36.
कार्बन के 2×108 परमाणु एक कतार में व्यवस्थित हैं। यदि इस व्यवस्था की लम्बाई 2.4 cm है तो कार्बन परमाणु के व्यास की गणना कीजिए।
उत्तर :
प्रश्न 37.
जिंक परमाणु का व्यास 2.6Å है—(क) जिंक परमाणु की त्रिज्या pm में तथा (ख) 1-6 cm की लम्बाई में कतार में लगातार उपस्थित परमाणुओं की संख्या की गणना कीजिए।
उत्तर :
प्रश्न 38.
किसी कण का स्थिर विद्युत आवेश 2.5×10-16c है। इसमें उपस्थित इलेक्ट्रॉनों की संख्या की गणना कीजिए।
उत्तर :
प्रश्न 39.
मिलिकन के प्रयोग में तेल की बूंद पर चमकती x-किरणों द्वारा प्राप्त स्थैतिक विद्युत-आवेश प्राप्त किया जाता है। तेल की बूंद पर यदि स्थैतिक विद्युत-आवेश
-1. 282 x 10-18c है तो इसमें उपस्थित इलेक्ट्रॉनों की संख्या की गणना कीजिए।
उत्तर :
इलेक्ट्रॉन द्वारा लिया गया आवेश = -1.6022×10-19C
∴ तेल की बूंद पर उपस्थित इलेक्ट्रॉनों की संख्या =
प्रश्न 40.
रदरफोर्ड के प्रयोग में सोने, प्लैटिनम आदि भारी परमाणुओं की पतली पन्नी पर ए-कणों द्वारा बमबारी की जाती है। यदि ऐलुमिनियम आदि जैसे हल्के परमाणु की पतली पन्नी ली जाए तो उपर्युक्त परिणामों में क्या अन्तर होगा?
उत्तर :
हल्के परमाणुओं जैसे एलुमिनियम के नाभिक छोटे तथा कम धन आवेश युक्त होते हैं। यदि | इनका प्रयोग रदरफोर्ड के प्रयोग में 0-कणों द्वारा बमबारी के लिए किया जाये तो नाभिकों के छोटे होने के कारण अधिकतर -कण लक्ष्य परमाणुओं से बिना टकराये ही बाहर निकल जायेंगे। जो कण नाभिक से टकरायेगें वे भी कम नाभिकीय आवेश के कारण अधिक विचलित नहीं होंगे।
प्रश्न 41.
तथा 79Br प्रतीक मान्य हैं, जबकि
तथा 35Br मान्य नहीं हैं। संक्षेप में कारण बताइए।
उत्तर :
एक तत्त्व के लिए परमाणु संख्या को मान स्थिर होता है, लेकिन द्रव्यमान संख्या का मान तत्त्व के समस्थानिक की प्रकृति पर निर्भर करता है। अतः द्रव्यमान संख्या को प्रतीक के साथ दर्शाना आवश्यक हो जाती है। परम्परा के अनुसार तत्त्व के प्रतीक में द्रव्यमान संख्या को ऊपर बायें तथा परमाणु संख्या को नीचे दायें ओर इस प्रकार लिखा जाता है- AXZ,
प्रश्न 42.
एक 81 द्रव्यमान संख्या वाले तत्व में प्रोटॉनों की तुलना में 31.7% न्यूट्रॉन अधिक हैं। इसका परमाणु प्रतीक लिखिए।
उत्तर :
दिये गये तत्त्व की द्रव्यमान संख्या = 81
प्रश्न 43.
37 द्रव्यमान संख्या वाले एक आयन पर ऋणावेश की एक इकाई है। यदि आयन में इलेक्ट्रॉन की तुलना में न्यूट्रॉन 11.1% अधिक है तो आयन का प्रतीक लिखिए।
उत्तर :
माना कि आयन में उपस्थित इलेक्ट्रॉनों की संख्या x है।
प्रश्न 44.
56 द्रव्यमान संख्या वाले एक आयन पर धनावेश की 3 इकाई हैं और इसमें इलेक्ट्रॉन की तुलना में 30.4% न्यूट्रॉन अधिक हैं। इस आयन का प्रतीक लिखिए।
उत्तर :
प्रश्न 45.
निम्नलिखित विकिरणों के प्रकारों को आवृत्ति के बढ़ते हुए क्रम में व्यवस्थित कीजिए
(क) माइक्रोवेव ओवन (oven) से विकिरण
(ख) यातायात-संकेत से त्रणमणि (amber) प्रकाश
(ग) एफ०एम० रेडियो से प्राप्त विकिरण
(घ) बाहरी दिक् से कॉस्मिक किरणें ।
(ङ) x-किरणें।
उत्तर :
FM < माइक्रोवेव < एम्बर प्रकाश <X-किरणें < कॉस्मिक किरणें।
प्रश्न 46.
नाइट्रोजन लेजर 337.1 nm की तरंगदैर्ध्य पर एक विकिरण उत्पन्न करती है। यदि उत्सर्जित फोटॉनों की संख्या 5.6 x 10-24 हो तो इस लेजर की क्षमता की गणना कीजिए।
उत्तर :
विकिरण की तरंगदैर्घ्य
λ = 337.1nm= 337.1×10-9m
प्रश्न 47.
निऑन गैस को सामान्यतः संकेत बोर्डों में प्रयुक्त किया जाता है। यदि यह 616 nm पर प्रबलता से विकिरण-उत्सर्जन करती है तो
(क) उत्सर्जन की आवृत्ति,
(ख) 30 सेकण्ड में इस विकिरण द्वारा तय की गई दूरी,
(ग) क्वाण्टम की ऊर्जा तथा
(घ) उपस्थित क्वाण्टम की संख्या की गणना कीजिए। (यदि यह 2J की ऊर्जा उत्पन्न करती है)।
उत्तर :
प्रश्न 48.
खगोलीय प्रेक्षणों में दूरस्थ तारों से मिलने वाले संकेत बहुत कमजोर होते हैं। यदि फोटॉन संसूचक 600 nm के विकिरण से कुल 3.15×10-18 J प्राप्त करता है तो संसूचक द्वारा प्राप्त फोटॉनों की संख्या की गणना कीजिए।
उत्तर :
प्रश्न 49.
उत्तेजित अवस्थाओं में अणुओं के जीवनकाल का माप प्रायः लगभग नैनो-सेकण्ड परास वाले विकिरण स्रोत का उपयोग करके किया जाता है। यदि विकिरण स्रोत का काल 2ns और स्पन्दित विकिरण स्रोत के दौरान उत्सर्जित फोटॉनों की संख्या 2.5×10-15 है तो स्रोत की ऊर्जा की गणना कीजिए।
उत्तर :
प्रश्न 50.
सबसे लम्बी द्विगुणित तरंगदैर्घ्य जिंक अवशोषण संक्रमण 589 और 589.6 nm पर देखा ‘. जाता है। प्रत्येक संक्रमण की आवृत्ति और दो उत्तेजित अवस्थाओं के बीच ऊर्जा के अन्तर की गणना कीजिए।
उत्तर :
प्रथम संक्रमण के लिए :
प्रश्न 51.
सीजियम परमाणु का कार्यफलन 1.9 ev है तो
(क) उत्सर्जित विकिरण की देहली तरंगदैर्घ्य,
(ख) देहली आवृत्ति की गणना कीजिए।
यदि सीजियम तत्व को 500 pm की तरंगदैर्घ्य के साथ विकीर्णित किया जाए तो निकले हुए फोटो इलेक्ट्रॉन की गतिज ऊर्जा और वेग की गणना कीजिए।
उत्तर :
प्रश्न 52.
जब सोडियम धातु को विभिन्न तरंगदैर्यों के साथ विकीर्णित किया जाता है तो निम्नलिखित परिणाम प्राप्त होते है-
λ (nm) : 500 450 400
vx10-5 (cm s-1) : 2.55 4.35 5.35
देहली तरंगदैर्घ्य तथा प्लांक स्थिरांक की गणना कीजिए।
उत्तर :
प्रश्न 53.
प्रकाश-विद्युत प्रभाव प्रयोग में सिल्वर धातु से फोटो इलेक्ट्रॉन का उत्सर्जन 0.35V की वोल्टता द्वारा रोका जा सकता है। जब 256.7 nm के विकिरण का उपयोग किया जाता है तो सिल्वर धातु के लिए कार्यफलन की गणना कीजिए।
उत्तर :
प्रश्न 54.
यदि 150 pm तरंगदैर्घ्य का फोटॉन एक परमाणु से टकराता है और इसके अन्दर बँधा हुआ इलेक्ट्रॉन 1.5×107 ms-1 वेग से बाहर निकलता है तो उस ऊर्जा की गणना कीजिए जिससे यह नाभिक से बँधा हुआ है।
उत्तर :
प्रश्न 55.
पाश्चन श्रेणी का उत्सर्जन संक्रमण ॥ कक्ष से आरम्भ होता है। कक्ष n=3 में समाप्त होता है तथा इसे= 3.29 x 1015(Hz) से दर्शाया जा सकता है। यदि संक्रमण 1285 nm पर प्रेक्षित होता है तो के मान की गणना कीजिए तथा स्पेक्ट्रम का क्षेत्र बताइए।
उत्तर :
प्रश्न 56.
उस उत्सर्जन संक्रमण के तरंगदैर्घ्य की गणना कीजिए, जो 1.3225 pm त्रिज्या वाले कक्ष से आरम्भ और 211.6 pm पर समाप्त होता है। इस संक्रमण की श्रेणी का नाम और स्पेक्ट्रम का क्षेत्र भी बताइए।
उत्तर :
मानते हुए कि निहित प्रतिदर्श एक H परमाणु है, nth कक्ष की त्रिज्या
प्रश्न 57.
दे-ब्रॉग्ली द्वारा प्रतिपादित द्रव्य के दोहरे व्यवहार से इलेक्ट्रॉन सूक्ष्मदर्शी की खोज हुई, जिसे जैव अणुओं और अन्य प्रकार के पदार्थों की अति आवधित प्रतिबिम्ब के लिए उपयोग में लाया जाता है। इस सूक्ष्मदर्शी में यदि इलेक्ट्रॉन का वेग 1.6×10-ms-1 है। तो इस इलेक्ट्रॉन से सम्बन्धित दे-ब्रॉग्ली तरंगदैर्घ्य की गणना कीजिए।
उत्तर :
प्रश्न 58.
इलेक्ट्रॉन विवर्तन के समान न्यूट्रॉन विवर्तन सूक्ष्मदर्शी को अणुओं की संरचना के निर्धारण में प्रयुक्त किया जाता है। यदि यहाँ 800 pm की तरंगदैर्घ्य ली जाए तो न्यूट्रॉन से सम्बन्धित अभिलाक्षणिक वेग की गणना कीजिए।
उत्तर :
प्रश्न 59.
यदि बोर के प्रथम कक्ष में इलेक्ट्रॉन का वेग 2.9 x106 ms-1 है तो इससे सम्बन्धित दे-ब्रॉग्ली तरंगदैर्घ्य की गणना कीजिए।
उत्तर :
प्रश्न 60.
एक प्रोटॉन, जो 1000v के विभवान्तर में गति कर रहा है, से सम्बन्धित वेग 4.37×105 ms-1 है। यदि 0.1 kg द्रव्यमान की हॉकी की गेंद इस वेग से गतिमान है तो इससे सम्बन्धित तरंगदैर्घ्य की गणना कीजिए।
उत्तर :
प्रश्न 61.
यदि एक इलेक्ट्रॉन की स्थिति + 0.002 nm की शुद्धता से मापी जाती है तो इलेक्ट्रॉन के संवेग में अनिश्चितता की गणना कीजिए। यदि इलेक्ट्रॉन का संवेगpm है तो । क्या इस मान को निकालने में कोई कठिनाई होगी?
उत्तर :
प्रश्नानुसार, Ax= 0.002nm=2×10-12m
हाइजेनबर्ग के अनिश्चितता के सिद्धान्त के अनुसार,
वास्तविक संवेग को परिभाषित नहीं किया जा सकता है क्योंकि यह संवेग में अनिश्चितता (Ap) से छोटा है।
प्रश्न 62.
छः इलेक्ट्रॉनों की क्वाण्टम संख्याएँ नीचे दी गई हैं। इन्हें ऊर्जा के बढ़ते क्रम में व्यवस्थित कीजिए। क्या इनमें से किसी की ऊर्जा समान है?
उत्तर :
दिये गये इलेक्ट्रॉन कक्षक 1.4d, 2. 3d, 3.4p, 4. 3d, 5. 3p तथा 6.4p से सम्बन्धित हैं। इनकी ऊर्जा इस क्रम में होगी-
5<2=4<6=3<1
प्रश्न 63.
ब्रोमीन परमाणु में 35 इलेक्ट्रॉन होते हैं। इसके 2p कक्षक में छः इलेक्ट्रॉन, 3p कक्षक में छः इलेक्ट्रॉन तथा 4p कक्षक में पाँच इलेक्ट्रॉन होते हैं। इनमें से कौन-सा इलेक्ट्रॉन न्यूनतम प्रभावी नाभिकीय आवेश अनुभव करता है?
उत्तर :
4p इलेक्ट्रॉन्स न्यूनतम प्रभावी नाभिकीय आवेश अनुभव करते हैं, क्योंकि ये नाभिक से सबसे अधिक दूर हैं।
प्रश्न 64.
निम्नलिखित में से कौन-सा कक्षक उच्च प्रभावी नाभिकीय आवेश अनुभव करेगा?
(i) 2s और 3s,
(ii) 44 और 4 तथा
(iii) 3d और 3p.
उत्तर :
(i) 25 कक्षक, 3s कक्षक की तुलना में नाभिक के अधिक निकट होगा। अत: 25 कक्षक उच्च प्रभावी नाभिकीय आवेश अनुभव करेगा।
(ii) d कक्षक, / कक्षकों की तुलना में अधिक भेदक (penetrating) होते हैं। इसलिए 44 कक्षक उच्च प्रभावी नाभिकीय आवेश अनुभव करेगा।
(iii) p कक्षक, 4 कक्षकों की तुलना में अधिक भेदक (penetrating) होते हैं। इसलिए, 3p कक्षक उच्च प्रभावी नाभिकीय आवेश अनुभव करेगा।।
प्रश्न 65.
Al तथा Si में 3p कक्षक में अयुग्मित इलेक्ट्रॉन होते हैं। कौन-सा इलेक्ट्रॉन नाभिक से अधिक प्रभावी नाभिकीय आवेश अनुभव करेगा?
उत्तर :
सिलिकॉन (+14) में, ऐलुमिनियम (+13) की तुलना में अधिक नाभिकीय आवेश होता है। अत: सिलिकॉन में उपस्थित अयुग्मित 3p इलेक्ट्रॉन अधिक प्रभावी नाभिकीय आवेश अनुभव करेंगे।
प्रश्न 66.
इन अयुग्मित इलेक्ट्रॉनों की संख्या बताइए|
(क) P
(ख) Si
(ग) Cr
(घ) Fe
(ङ) Kr
उत्तर :
इन तत्त्वों के इलेक्ट्रॉनिक विन्यास तथा अयुग्मित इलेक्ट्रॉनों की संख्या निम्न है-
प्रश्न 67.
(क) n = 4 से सम्बन्धित कितने उपकोश हैं?
(ख) उस उपकोश में कितने इलेक्ट्रॉन उपस्थित होंगे जिसके लिए ms =-एवं ॥= 4हैं?
उत्तर :
परीक्षोपयोगी प्रश्नोत्तर
बहुविकल्पीय प्रश्न
प्रश्न 1.
कैथोड किरणों के लिए कौन-सा कथन असत्य है?
(i) सीधी रेखा में कैथोड की तरफ चलती हैं।
(ii) ऊष्मा उत्पन्न करती हैं।
(iii) ऋण आवेश रहता है।
(iv) उच्च परमाणु भार वाली धातु से टकराकर X-किरणें उत्पन्न करती हैं।
उत्तर :
(i) सीधी रेखा में कैथोड की तरफ चलती हैं।
प्रश्न 2.
न्यूट्रॉन एक मौलिक कण है जिसमें
(i) +1 आवेश एवं एक इकाई द्रव्यमान होता है।
(ii) 0 आवेश एवं एक इकाई द्रव्यमान होता है।
(iii) 0 आवेश एवं 0 द्रव्यमान होता है।
(iv) -1 आवेश एवं इकाई द्रव्यमान होता है।
उत्तर :
(ii) 0 आवेश एवं एक इकाई द्रव्यमान होता है।
प्रश्न 3.
किसी तत्व के 3d उपकोश में 7 इलेक्ट्रॉन हैं। तत्त्व का परमाणु क्रमांक है
(i) 24
(ii) 27
(iii) 28
(iv) 29
उत्तर :
(ii) 27
प्रश्न 4.
परमाणु क्रमांक 12 वांले तत्त्व में इलेक्ट्रॉनों की संख्या है।
(i) 0
(ii) 12
(iii) 6
(iv) 14
उत्तर :
(ii) 12
प्रश्न 5.
किसी तत्त्व के समस्थानिक ,xm में न्यूट्रॉनों की संख्या होगी
(i) m+n
(ii) m
(iii) n
(iv) m-n
उत्तर :
(iv) m-n
प्रश्न 6.
दे-ब्रॉग्ली के सिद्धान्त के अनुसार
(i) E= mc2
(ii)
(iii) ∆E= ∆h
(iv)
उत्तर :
(ii)
प्रश्न 7.
निश्चितता के सिद्धान्त के अनुसार
(i) E = mc2
(ii)
(iii)
(iv)
उत्तर :
(i)
प्रश्न 8.
निम्न में कौन-सा क्वाण्टम संख्याओं का समूह असम्भव है ?
या
किसी परमाणु में कौन-सी इलेक्ट्रॉनों की व्यवस्था सम्भव नहीं है?
(i) 3,2,-2,
(ii) 4, 0, 0,
(iii) 3, 2, 3,
(iv) 5,3, 0,
उत्तर :
(i) 3,2,-3,
प्रश्न 9.
3d3 निकाय के तीसरे इलेक्ट्रॉन की चारों क्वाण्टम संख्याओं का सही क्रम
(i) n = 3,1= 2, m= +3, s=
(ii) n = 3,l= 2, m= + 1, s=
(iii) n= 3, 1= 2, m= +2, s=
(iv) n = 3,1= 2, m= 0, s=
उत्तर :
(iv) n= 3, 1 = 2, m=0 s=
प्रश्न 10.
चुम्बकीय क्वाण्टम संख्या बताती है।
(i) ऑर्बिटलों की आकृति
(ii) ऑर्बिटलों का आकार
(iii) ऑर्बिटलों का अभिविन्यास
(iv) नाभिकीय स्थायित्व
उत्तर :
(iii) ऑर्बिटलों का अभिविन्यास
प्रश्न 11.
परमाणु उपकोशों की बढ़ती ऊर्जा का सही क्रम है।
(i) 5p<4f< 6s< 5d
(ii) 5p< 6s<4f<5d
(iii) 4f<5p<5d<6s
(iv) 5p<5d <4f< 6s
उत्तर :
(ii) 5p<6s<4f<5d
प्रश्न 12.
ताँबा परमाणु की आद्य अवस्था में इलेक्ट्रॉनिक विन्यास है।
(i) [Ar] 3d94s2
(ii) [Ar] 3d104s2
(iii) [Ar] 3d104s1 ,
(iv) [Ar] 3d104s2 4p1
उत्तर :
(iii) [Ar] 3d104s1
प्रश्न 13.
Fe3+ (परमाणु क्रमांक Fe=26) का सही विन्यास है।
(i) 1s2, 2s2, 3s2 3p6 3d5
(ii) 1s2, 2s2 2p6, 3s2 3p6 3d6, 4s2
(iii) 1s2, 2s2 2p6, 3s2 3p63d5, 4s2
(iv) 1s2 ,2s2 2p6, 3s2 3p6 3d5 4s1
उत्तर :
(i)s2, 2s2, 3s2 3p6 3d5
प्रश्न 14.
Cr परमाणु (Z = 24) की तलस्थ अवस्था में सही इलेक्ट्रॉनिक विन्यास है।
(i) [Ar] 3d4,4s2
(ii) [Ar] 3d5,4s2
(iii) [Ar] 3d6,4s2
(iv) [Ar] 3d5,4s1
उत्तर :
(iv)[Ar] 3d6,4s1
प्रश्न 15.
Fe2+(z= 26) में 4-इलेक्ट्रॉनों की संख्या के बराबर नहीं है।
(i) Ne (Z=10) में p-इलेक्ट्रॉनों की संख्या
(ii) Mg (Z= 12) में इलेक्ट्रॉनों की संख्या
(iii) Fe में d-इलेक्ट्रॉनों की संख्या
(iv) Cl–(Z=17) में p-इलेक्ट्रॉनों की संख्या
उत्तर :
(iv)Cl–(2=17) में p-इलेक्ट्रॉनों की संख्या
प्रश्न 16.
H– का इलेक्ट्रॉनिक विन्यास है।
(i) 1s0
(ii) 1s1
(iii) 1s2
(iv) 1s2, 2s1
उत्तर :
(iii) H– में 2 इलेक्ट्रॉन हैं, अत: विकल्प (iii) 1s2 सही है।
प्रश्न 17.
निम्न आयनों में कौन अनुचुम्बकीय है?
(i) Zn2+
(ii) Ni2+
(iii) Cu2+
(iv) Ca2+
उत्तर :
(ii) एवं (iii)
प्रश्न 18.
प्रतिचुम्बकीय आयन है।
(i) Cu2+
(ii) Fe2+
(iii) Ni2+
(iv) Zn2+
उत्तर :
(iv) Zn2+
प्रश्न 19.
(n+1) नियमानुसार इलेक्ट्रॉन np ऊर्जा स्तर पूर्ण करने के बाद
(i) (n-1)d में प्रवेश करता है।
(ii) (n+ 1)s में प्रवेश करता है।
(iii) (n+ 1)p में प्रवेश करता है।
(iv) nd में प्रवेश करता है।
उत्तर :
(ii) (n+1)s में प्रवेश करता है।
प्रश्न 20.
p ऑर्बिटलों में चारों इलेक्ट्रॉनों का सही वितरण है।
उत्तर :
प्रश्न 21.
Cu2+ (z=29) में अयुग्मित इलेक्ट्रॉनों की संख्या है।
(i) 1
(ii) 2
(iii) 3
(iv) 4
उत्तर :
(i) 1
प्रश्न 22.
निम्नलिखित में सेमान अयुग्मित इलेक्ट्रॉनों वाले आयनों को पहचानिए
I. . Fe3+ (Z=26)
II. Zn2+ (Z= 30)
III. Cr3+ (Z = 24)
IV. Mn2+ (2=25)
(i) I तथा II ।
(ii) I, II तथा III
(iii) I तथा III
(iv) I तथा IV
उत्तर :
(iv) I तथा IV
प्रश्न 23.
निम्न में से किसमें अयुग्मित इलेक्ट्रॉन नहीं हैं?
(i) Fe2+
(ii) Ni2+
(iii) Cu2+
(iv) Zn2+
उत्तर :
(iv) Zn2+
प्रश्न 24.
निम्नलिखित किस आयन में अयुग्मित इलेक्ट्रॉनों की संख्या अधिकतम है?
(i) Cr3+ (Z=24)
(ii) Ni2+ (Z= 28)
(iii) Mn2+ (Z=25)
(iv) Ti22+ (Z= 22)
उत्तर :
(iii) Mn2+ (Z= 25)
प्रश्न 25.
Ni2+(z = 28) आयन में अयुग्मित इलेक्ट्रॉनों की संख्या है।
(i) 1
(ii) 2
(iii) 3
(iv) 8
उत्तर :
(ii) 2
प्रश्न 26.
Cr2+ (2=24) आयन में अयुग्मित इलेक्ट्रॉनों की संख्या है।
(i) 6
(ii) 4
(iii) 3
(iv) 1
उत्तर :
(ii) 4
प्रश्न 27.
निम्नलिखित में से किस आयन में अयुग्मित इलेक्ट्रॉनों की संख्या शून्य (0) है?
(i) Cr22+ (2=24)
(ii) Fe2+(Z= 26)
(iii) Cu2+ (Z = 29)
(iv) Zn2+(Z= 30)
उत्तर :
(iv) Zn2+ (Z = 30)
प्रश्न 28.
कार्बन परमाणु में अयुग्मित इलेक्ट्रॉनों की संख्या है।
(i) 1
(ii) 4
(iii) 3
(iv) 2
उत्तर :
(iv) 2
प्रश्न 29.
आयन जिसमें सबसे अधिक अयुग्मित इलेक्ट्रॉन हैं, है।
(i) Fe3+
(ii) Co2+
(iii) Ni2+
उत्तर :
(i) Fe3+
अतिलघु उत्तरीय प्रश्न
प्रश्न 1.
दो कारण दीजिए जिनके आधार पर इलेक्ट्रॉन को पदार्थ का मौलिक कण समझा जाता है।
उत्तर :
इलेक्ट्रॉन सभी पदार्थों के मौलिक कण होते हैं। ऐसा कई प्रकार की घटनाओं के अध्ययन द्वारा सिद्ध हुआ है। इसके दो प्रमुख कारण निम्नलिखित हैं-
- तापायनिक उत्सर्जन-जब किसी पदार्थ को उच्च ताप तथा कम दाब पर गर्म किया जाता है। तब पदार्थ से इलेक्ट्रॉन बाहर निकलने लगते हैं।
- प्रकाश वैद्युत प्रभाव-जब X-किरणें, y-किरणे अथवा पराबैंगनी किरणें धातुओं से टकराती | हैं, तब भी इलेक्ट्रॉन उन धातुओं से बाहर निकलने लगते हैं।
प्रश्न 2.
इलेक्ट्रॉन की तरंग प्रवृतिं क्या है ? इससे सम्बन्धित व्यंजक लिखिए।
उत्तर :
सन् 1924 में दे-ब्रॉग्ली ने यह विचार प्रस्तुत किया कि गतिशील सूक्ष्म कण; जैसे—इलेक्ट्रॉन, प्रोटॉन आदि तरंग के गुण प्रदर्शित करते हैं। यदि m द्रव्यमान का एक सूक्ष्म कण ) वेग से गतिमान है, तो उसके तरंगदैर्घ्य 2 और संवेग p=) में निम्नलिखित सम्बन्ध होता है।
प्रश्न 3.
इलेक्ट्रॉन की द्वैती प्रकृति से आप क्या समझते हैं?
उत्तर :
इलेक्ट्रॉन, कण तथा तरंग दोनों के गुण व्यक्त करते हैं, इसे इलेक्ट्रॉन की द्वैती प्रकृति कहते हैं; जैसे
- कैथोड किरणें (जिनमें केवल इलेक्ट्रॉन होते हैं) अपने मार्ग में रखी हल्की वस्तु को चला | सकती हैं। इससे सिद्ध होता है कि इलेक्ट्रॉनों में कण के गुण हैं।
- प्रकाश किरणों की तरह इलेक्ट्रॉन किरणपुंज भी विवर्तन और व्यतिकरण प्रक्रिया प्रदर्शित करता है। इससे सिद्ध होता है कि इलेक्ट्रॉनों में तरंग के गुण हैं।
प्रश्न 4.
इलेक्ट्रॉन को ऋणात्मक आवेश की इकाई क्यों माना जाता है?
उत्तर :
इलेक्ट्रॉन पर उपस्थित आवेश विद्युत का सूक्ष्मतम आवेश होता है इसलिए इलेक्ट्रॉन के आवेश को इकाई ऋणावेश माना जाता है।
प्रश्न 5.
द्रव्यमान संख्या तथा परमाणु भार में सम्बन्ध स्पष्ट कीजिए।
उत्तर :
इलेक्ट्रॉन का द्रव्यमान लगभग नगण्य होता है तथा प्रोटॉन एवं न्यूट्रॉन का द्रव्यमान लगभग 1 amu होता है। अतः परमाणु भार और द्रव्यमान संख्या लगभग बराबर होती है।
परमाणु भार = द्रव्यमान संख्या
प्रश्न 6.
हाइजेनबर्ग का अनिश्चितता का नियम स्पष्ट कीजिए।
उत्तर :
इस नियम के अनुसार, किसी गतिशील कण की स्थिति तथा वेग दोनों का एक साथ यथार्थ निर्धारण सम्भव नहीं है।
यदि ∆x किसी कण की स्थिति निर्धारण की अनिश्चितता हो और ∆p उसके संवेग (द्रव्यमान x वेग) के निर्धारण की अनिश्चितता हो तो इस सिद्धान्त के अनुसार,
जहाँ h = प्लांक स्थिरांक (6.625×10-27 अर्ग-सेकण्ड)
प्रश्न 7.
हाइड्रोजन परमाणु का इलेक्ट्रॉन मेघ मॉडल समझाइए।
उत्तर :
आधुनिक विचारों के अनुसार, नाभिक के चारों ओर स्पष्ट वृत्तीय कक्षाएँ नहीं हैं, अपितु इलेक्ट्रॉन मेघ है। हाइड्रोजन परमाणु में उपस्थित इलेक्ट्रॉन का ऋणावेश एक मेघ (cloud) के रूप में नाभिक के चारों ओर विसरित रहता है। जिन क्षेत्रों में इलेक्ट्रॉन के उपस्थित होने की प्रायिकता अधिक होती है, उन क्षेत्रों में ऋणावेशित इलेक्ट्रॉन मेघ का घनत्व अधिक होता है। वे त्रिविम क्षेत्र, जिनमें निश्चित ऊर्जा के इलेक्ट्रॉन के उपस्थित होने की प्रायिकता अधिकतम होती है, ऑर्बिटल (कक्षक) कहलाते हैं। भिन्न-भिन्न उपकोशों में कक्षकों की संख्याएँ भिन्न-भिन्न होती हैं।
प्रश्न 8.
कोश एवं उपकोश क्या हैं?
उत्तर :
समान मुख्य क्वाण्टम संख्या n के परमाणु कक्षकों का समूह कोश कहलाता है जबकि समान मुख्य क्वाण्टम संख्या n की और दिगंशी क्वाण्टम संख्या । के परमाणु कक्षकों का समूह उपकोश कहलाता है।
प्रश्न 9.
कक्षक किसे कहते हैं? एक कक्षक में अधिकतम कितने इलेक्ट्रॉन रह सकते हैं?
उत्तर :
कक्षक नाभिक के चारों ओर स्थित आकाश के उन त्रिविम क्षेत्रों को कहते हैं जिनमें इलेक्ट्रॉन औसतन अधिक पाए जाते हैं। प्रत्येक कक्षक का केन्द्र परमाणु का नाभिक होता है। एक कक्षक में अधिकतम दो इलेक्ट्रॉन रह सकते हैं जिनके चक्रण विपरीत दिशा में होते हैं।
प्रश्न 10.
d-उपकोश में पाँच कक्षक होते हैं। स्पष्ट कीजिए।
उत्तर :
d-उपकोश में अधिकतम इलेक्ट्रॉनों की संख्या 10 होती है, जबकि एक कक्षक में केवल ” अधिकतम दो इलेक्ट्रॉन रह सकते हैं, अतः 4-उपकोश में पाँच कक्षक होते हैं।
प्रश्न 11.
एक तत्त्व के 47 उपकोश में 7 इलेक्ट्रॉन हैं। इस / उपकोश के अन्तिम इलेक्ट्रॉन की चारों क्वाण्टम संख्याएँ लिखिए।
उत्तर :
प्रश्न 12.
क्लोरीन के अन्तिम इलेक्ट्रॉन के लिए चारों क्वाण्टम संख्याओं के मान लिखिए।
उत्तर :
प्रश्न 13.
एक तत्त्व (परमाणु क्रमांक = 21) के अन्तिम डाले गये इलेक्ट्रॉन के लिए चारों क्वाण्टम संख्याओं के मान ज्ञात कीजिए।
उत्तर :
प्रश्न 14.
मुख्य क्वाण्टम संख्या 2 के लिए सभी चुम्बकीय क्वाण्टम संख्याओं के मान लिखिए।
उत्तर :
प्रश्न 15.
3d8 इलेक्ट्रॉन के लिए #, 1, तथा s के मान लिखिए।
उत्तर :
प्रश्न 16.
Fe (Z = 26) के 24 वें इलेक्ट्रॉन के लिए क्वाण्टम संख्याओं के मान लिखिए।
उत्तर :
-Fe (Z = 26) का इलेक्ट्रॉनिक विन्यास निम्नवत् है-
प्रश्न 17.
Sc (परमाणु क्रमांक =210) में अन्तिम इलेक्ट्रॉन के लिए चारों क्वाण्टम संख्याओं के मान लिखिए।
उत्तर :
Sc (Z = 21) तत्त्व का इलेक्ट्रॉनिक विन्यास निम्नवत् है-
प्रश्न 18.
L कोश में कितने उपकोश होते हैं। इसके उपकोशों की आकृतियाँ तथा अभिविन्यास बताइए।
उत्तर :
प्रश्न 19.
s, p और 4 कक्षकों की आकृतियाँ बताइए?
उत्तर :
कक्षक की आकृति गोलाकार, p कक्षक की आकृति डम्बलाकार तथा d कक्षक की आकृति द्वि-डम्बलाकार होती है।
प्रश्न 20.
ऑफबाऊ सिद्धान्त का उल्लेख कीजिए।
उत्तर :
इस सिद्धान्त के अनुसार, “विभिन्न कक्षकों में इलेक्ट्रॉनों का प्रवेश उपकोशों की ऊर्जा की वृद्धि के क्रमानुसार होता है. और इलेक्ट्रॉन एक-एक करके ऊर्जा के बढ़ते क्रम वाले उपकक्षकों में प्रवेश पाते हैं।”
प्रश्न 21.
पाउली के अपवर्जन नियम को स्पष्ट कीजिए तथा एक परमाणु के चतुर्थ मुख्य ऊर्जा स्तर में इलेक्ट्रॉनों की अधिकतम संख्या की गणना कीजिए।
उत्तर :
इस सिद्धान्त के अनुसार, “किसी परमाणु में दो इलेक्ट्रॉनों के लिए चारों क्वाण्टम संख्याओं के मान समान नहीं हो सकते हैं। यदि किन्हीं दो इलेक्ट्रॉनों के लिए n, 1 तथा m के मान समान भी हो जायें, तो s का मान निश्चित रूप से भिन्न होगा। इस स्थिति में यदि प्रथम इलेक्ट्रॉन के लिए ” कामान हो, तो दूसरे इलेक्ट्रॉन के लिए यह मान
होगा। परमाणु के चतुर्थ मुख्य ऊर्जा स्तर में इलेक्ट्रॉनों की अधिकतम संख्या = 2n2 = 2×16= 32
प्रश्न 22.
हुण्ड के नियम का उल्लेख कीजिए। एक उदाहरण देकर इसे स्पष्ट कीजिए।
उत्तर :
हुण्ड के नियम के अनुसार, “किसी उपकोश के कक्षक में इलेक्ट्रॉन तभी युग्मित होते हैं जब उस उपकोश के सभी कक्षकों में एक-एक इलेक्ट्रॉन भर जाता है। इलेक्ट्रॉन जब युग्मित होते हैं तो युग्म के दोनों इलेक्ट्रॉन विपरीत चक्रण वाले होते हैं।”
इस नियम के अनुसार, इ-कक्षक में दूसरे इलेक्ट्रॉन के प्रवेश पर, p-कक्षक में चौथे इलेक्ट्रॉन के प्रवेश । पर, 4-कक्षक में छठे इलेक्ट्रॉन के प्रवेश पर तथा f-कक्षक में आठवें इलेक्ट्रॉन के प्रवेश पर युग्मन आरम्भ होता है। उदाहरणार्थ-नाइट्रोजन परमाणु में p-उपकोश में तीनों इलेक्ट्रॉन अलग-अलग । p-कंक्षकों अर्थात् px, py और pz में रहते हैं। ये इलेक्ट्रॉन अयुग्मित तथा समदिश चक्रण वाले होते हैं।
इस परमाणु में इलेक्ट्रॉन वितरण इस प्रकार होता है।
प्रश्न 23.
किसी तत्त्व के 34 उपकोश में 4 इलेक्ट्रॉन हैं। तत्त्व के 4 उपकोश में इलेक्ट्रॉनों का वितरण प्रदर्शित कीजिए।
उत्तर :
हुण्ड के नियमानुसार, इलेक्ट्रॉनों का वितरण निम्नवत् होगा-
प्रश्न 24.
Cu2+तथा Mn4+का इलेक्ट्रॉनिक विन्यास s, p, 4, f में लिखिए।
(Cu की परमाणु संख्या = 29, Mn की परमाणु संख्या = 25)
उत्तर :
प्रश्न 25.
एक तत्त्व के बाह्यतम कोश का इलेक्ट्रॉनिक विन्यास 4s2 4p5 है। इस तत्त्व का पूर्ण | इलेक्ट्रॉनिक विन्यास लिखिए। इस तत्त्व का परमाणु क्रमांक क्या है ?
उत्तर :
प्रश्न 26.
मैग्नीशियम, कैल्सियम तथा ब्रोमीन के परमाणु क्रमांक क्रमशः 25, 20 तथा 35 हैं। निम्नलिखित के इलेक्ट्रॉनिक विन्यास लिखिए Mn2+,ca2+ तथा Br-1
उत्तर :
प्रश्न 27.
Fe2+ का इलेक्ट्रॉनिक विन्यास और अयुग्मित इलेक्ट्रॉनों की संख्या लिखिए।
(Z =26)
उत्तर :
प्रश्न 28.
कोबाल्ट (Z = 27) का इलेक्ट्रॉनिक विन्यास लिखिए एवं उसमें उपस्थित अयुग्मित | इलेक्ट्रॉनों की संख्या बताइए।
उत्तर :
प्रश्न 29.
किसी परमाणु के 7 उपकोश में दस इलेक्ट्रॉन हैं। इनका बॉक्स वितरण दिखाते हुए अयुग्मित इलेक्ट्रॉनों की संख्या बताइए। अपने उत्तर का आधार स्पष्ट कीजिए।
उत्तर :
प्रश्न 30.
क्रोमियम (Cr) का परमाणु क्रमांक 24 है। Cr3+ का इलेक्ट्रॉनिक विन्यासs, p, d,f के | रूप में दीजिए तथा अयुग्मित इलेक्ट्रॉनों की संख्या बताइए।
उत्तर :
लघु उत्तरीय प्रश्न
प्रश्न 1.
इलेक्ट्रॉन, प्रोटॉन एवं न्यूट्रॉन की खोज किसने की? इन कणों के अभिलक्षण भी लिखिए।
उत्तर :
इलेक्ट्रॉन-इलेक्ट्रॉन अति सूक्ष्म ऋणावेशित कण हैं। एक इलेक्ट्रॉन पर इकाई ऋणावेश होता है। इलेक्ट्रॉन का द्रव्यमान (me = 5.4860×10-4 amu) हाइड्रोजन परमाणु (H) के द्रव्यमान (mh = 100797amu) का लगभग है। इलेक्ट्रॉन की खोज सन् 1897 में अंग्रेज वैज्ञानिक जे०जे० टॉमसन ने कैथोड किरणों में की। सभी परमाणुओं में इलेक्ट्रॉन होते हैं। प्रोटॉन-प्रोटॉन अति सूक्ष्म धनावेशित कण हैं। एक प्रोटॉन पर इकाई धनावेश होता है।
प्रोटॉन का द्रव्यमान (mp = 1.007276amu) हाइड्रोजन परमाणु (H) के द्रव्यमान के लगभग बराबर है। हाइड्रोजन परमाणु में से इलेक्ट्रॉन बाहर निकल जाने पर जो इकाई धनावेशित कण (H+) शेष रह जाता है उसे हाइड्रोजन परमाणु का नाभिक या प्रोटॉन कहते हैं। अंग्रेज भौतिक विज्ञानी अर्नेस्ट रदरफोर्ड (191) ने प्रोटॉन की खोज की और सिद्ध किया कि सभी परमाणुओं में प्रोटॉन होते हैं।
न्यूट्रॉन-न्यूट्रॉन विद्युत् उदासीन कण हैं। न्यूट्रॉन का द्रव्यमाने (mn = 1.008665 amu) हाइड्रोजन परमाणु (H) के द्रव्यमान के लगभग बराबर है। न्यूट्रॉन की खोज सन् 1932 में अंग्रेज वैज्ञानिक जे० चैडविक ने की। हाइड्रोजन-1 परमाणु () को छोड़कर अन्य सभी परमाणुओं में न्यूट्रॉन होते हैं।
प्रश्न 2.
टॉमसन का परमाणु मॉडल समझाइए। इसकी सीमाएँ भी लिखिए।
उत्तर :
टॉमसन का परमाणु मॉडल ।। कैथोड किरणों और धन किरणों पर किए गए प्रयोगों से प्राप्त जानकारी के आधार पर जे०जेटॉमसन (J.J. Thomson, 1904) ने प्रथम परमाणु मॉडल प्रस्तुत किया। टॉमसन मॉडल के अनुसार, परमाणु अतिसूक्ष्म गोलाकार (spherical) विद्युत-उदासीन कण हैं जो धन और ऋण आवेशित द्रव्य से बने हुए हैं। धनावेशित द्रव्य परमाणु में एक समान रूप से फैला हुआ है तथा इलेक्ट्रॉन धन-आवेश में इस प्रकार पॅसे हुए हैं जैसे तरबूज में बीज धंसे रहते हैं।
टॉमसन परमाणु मॉडल, परमाणु का “तरबूज मॉडल” (water-melon model) भी कहलाता है। यह मॉडल परमाणु स्पेक्ट्रम की उत्पत्ति की व्याख्या करने में असफल रहा। सन् 1911 में लॉर्ड रदरफोर्ड ने ऐल्फा-कणों के प्रकीर्णन प्रयोग द्वारा इस मॉडल का खण्डन किया और परमाणु का नाभिकीय मॉडल प्रस्तुत किया।
प्रश्न 3.
परमाणु क्रमांक से आप क्या समझते हैं?
उत्तर :
किसी तत्व के परमाणु नाभिक पर स्थित धनावेश इकाइयों की संख्या को उस तत्व का परमाणु क्रमांक (2) कहते हैं। परमाणु नाभिक पर स्थित धनावेश इकाइयों की संख्या नाभिक में उपस्थित प्रोटॉनों की संख्या के बराबर होती है। अत: किसी तत्व के परमाणु नाभिक में उपस्थित प्रोटॉनों की संख्या उस तत्व का परमाणु क्रमांक (Z) होता है। प्रत्येक तत्व का परमाणु क्रमांक निश्चित और स्थिर होता है। भिन्न-भिन्न तत्वों के परमाणु क्रमांक भिन्न-भिन्न होते हैं। किसी तत्व के सभी परमाणुओं में प्रोटॉनों की संख्या समान होती है। अतः परमाणु क्रमांक (2) तत्वों का मूल लक्षण (fundamental property) है। हाइड्रोजन का परमाणु क्रमांक 1 है, इस कथन से यह अभिप्राय है कि हाइड्रोजन परमाणु के नाभिक में एक प्रोटॉन है। कार्बन का परमाणु क्रमांक 6 और सोडियम का परमाणु क्रमांक 11 है।
प्रश्न 4.
निम्नलिखित को स्पष्ट कीजिए।
(i) समस्थानिक,
(ii) समभारिक
उत्तर :
(i) समस्थानिक–किसी एक तत्त्व के ऐसे परमाणु जिनकी परमाणु संख्या समान होती है। परन्तु द्रव्यमान संख्या भिन्न होती है, समस्थानिक कहलाते हैं। ऐसे परमाणुओं में प्रोटॉनों की संख्या तो समान होती है परन्तु न्यूट्रॉनों की संख्या भिन्न होती है। उदाहरणार्थ-प्रोटियम (1H1), ड्यूटीरियम (1H2) तथा ट्राइटियम (1H3) हाइड्रोजन के तीन समस्थानिक हैं। इन समस्थानिकों की परमाणु संख्या 1 है। परन्तु द्रव्यमान संख्याएँ क्रमशः 1, 2 व 3 हैं।
(ii) समभारिक–विभिन्न तत्त्वों के ऐसे परमाणु जिनकी द्रव्यमान संख्या समान होती है, समभारिक कहलाते हैं। उदाहरणार्थ- 18Ar40, 19K40 तथा 20Ca40 समभारिक हैं।
प्रश्न 5.
निम्न में से कौन-से इलेक्ट्रॉनिक विन्यास नियमानुसार सही नहीं हैं। सम्बन्धित नियमों को परिभाषित भी कीजिए
(i) 1s2, 2s2
(ii) 1s2, 2s2, 2p2x, 2p1y
(iii) 1s2, 2s2, 2p2x, 2p2y , 2p1z
(iv) 1s2, 2s2, 2p7
उत्तर :
(ii) 1s2,2s2,2p2x,2p1y), इलेक्ट्रॉनिक विन्यास सही नहीं है, क्योंकि हुण्ड के नियमानुसार इसका सही विन्यास 1s2,2s2,2p1x,2p1y, 2p1z होना चाहिए। हुण्ड का नियम–किसी उपकोश के कक्षक, में इलेक्ट्रॉनों का युग्मन तब तक नहीं हो सकता जब तक प्रत्येक ऑर्बिटल में समदिश स्पिन के एक-एक इलेक्ट्रॉन नहीं हो जाते हैं।
(iv) 1s2,2s2,2p7 इलेक्ट्रॉनिक विन्यास सही नहीं है क्योंकि पाउली के अपवर्जन नियम के अनुसार, p उपकोश में अधिकतम 6 इलेक्ट्रॉन ही हो सकते हैं। सही इलेक्ट्रॉनिक विन्यास इस प्रकार होना चाहिए 1s2,2s2,2p6,3s1
पाउली का अपवर्जन नियम-“किसी परमाणु के किन्हीं दो इलेक्ट्रॉनों के लिए चारों क्वाण्टम संख्याओं के मान समान नहीं हो सकते हैं।”
विस्तृत उत्तरीय प्रश्न
प्रश्न 1.
रदरफोर्ड के परमाणु मॉडल (सिद्धान्त) का उल्लेख कीजिए। इसकी सीमाएँ भी लिखिए।
उत्तर :
रदरफोर्ड का परमाणु मॉडल (सिद्धान्त ) : विभिन्न तत्वों के परमाणुओं पर तीव्रगामी o-कणों की बमबारी के प्रयोग से प्राप्त प्रेक्षणों के आधार पर रदरफोर्ड ने निम्नलिखित सिद्धान्त दिया, जिसे परमाणु का नाभिकीय सिद्धान्त कहते हैं जो कि निम्न प्रकार है-
- परमाणु अति सूक्ष्म, गोलाकार, विद्युत-उदासीन कण है। यह धनावेशित नाभिक के चारों ओर विशाल त्रिविम आकाश में गतिशील इलेक्ट्रॉनों का एक समूह होता है।
- परमाणु का केन्द्रीय भाग, जिसमें परमाणु का कुल धनावेश और लगभग समस्त द्रव्यमान निहित होता है, नाभिक कहलाता है।
- नाभिक पर कुल केन्द्रित धनावेश, इलेक्ट्रॉनों के कुल ऋणावेशों के बराबर होता है जिससे परमाणु में विद्युत आवेशों का सन्तुलन बना रहता है और वह उदासीन रहता है।
- नाभिक की त्रिज्या 10-12 सेमी और परमाणु की त्रिज्या 10-8 सेमी होती है। स्पष्ट है कि परमाणु की त्रिज्या नाभिक की त्रिज्या से लगभग 10,000 गुना अधिक होती है।
- परमाणु के ऋणावेशित इलेक्ट्रॉन इसके धनावेशित नाभिक के चारों ओर चक्कर लगाते रहते हैं।
- परमाणु के नाभिक में स्थित धनावेशित कणों की संख्या उसके ऋणावेशित इलेक्ट्रॉनों की संख्या के बराबर होती है; अतः परमाणु विद्युत-उदासीन होता है।
- नाभिक तथा उसके चारों ओर भ्रमण कर रहे इलेक्ट्रॉन के बीच परस्पर स्थिर-वैद्युत आकर्षण होने के बाद भी इलेक्ट्रॉन तीब्र गति से भ्रमण करते रहते हैं और नाभिक में नहीं गिरते; क्योंकि इन इलेक्ट्रॉनों के परिक्रमण से उत्पन्न अपकेन्द्री बल नाभिक के स्थिर-वैद्युत आकर्षण बल को सन्तुलित कर देता है।
रदरफोर्ड के उपर्युक्त मॉडल को परमाणु का मॉडल (nuclear model) कहा गया। इस मॉडल को सौर (solar) या ग्रहीय (planetary) मॉडल भी कहते हैं; क्योंकि इस मॉडल में यह कल्पना की गई है कि जिस प्रकार सूर्य के चारों ओर ग्रह परिक्रमा करते हैं; उसी प्रकार नाभिक के चारों ओर इलेक्ट्रॉन घूमते रहते हैं। रदरफोर्ड के परमाणु मॉडल की सीमाएँ (अर्थात् दोष या कमियाँ) निम्नलिखित हैं-
- रदरफोर्ड के परमाणु मॉडल के अनुसार इलेक्ट्रॉन नाभिक के चारों ओर विभिन्न कक्षाओं में तीव्र गति से चक्कर लगाते हैं। क्लार्क मैक्सवेल ने बताया कि विद्युत-चुम्बकीय सिद्धान्त के अनुसार, ऋणावेशित इलेक्ट्रॉनों को धनावेशित नाभिक के चारों ओर चक्कर लगाने के कारण सतत रूप से प्रकाश विकिरण उत्सर्जित करने चाहिए जिससे लगातार ऊर्जा की क्षति होनी चाहिए तथा उनकी कक्षा की त्रिज्या लगातार कम होती जानी चाहिए और अन्त में वे नाभिक में गिरकर नष्ट हो जाने चाहिए। परन्तु ऐसा नहीं होता है क्योंकि परमाणु एक स्थायी निकाय है। अतः रदरफोर्ड मॉडल परमाणु निकाय के स्थायित्व की व्यवस्था करने में असफल रहा है।
- रदरफोर्ड के -कणों के प्रकीर्णन प्रयोग से परमाणु में उपस्थित प्रोटॉनों तथा इलेक्ट्रॉनों की । | संख्या के बारे में कोई जानकारी प्राप्त नहीं होती है। अतः यह परमाणु संरचना के बारे में कुछ भी स्पष्ट नहीं करता है।
- इस सिद्धान्त के द्वारा यह भी स्पष्ट नहीं होता कि इलेक्ट्रॉन नाभिक के चारों ओर कहाँ और कैसे स्थित रहता है और उसकी ऊर्जा क्या है।
- परमाणु रेखीय स्पेक्ट्रम (line spectrum) देते हैं, जबकि यदि इलेक्ट्रॉन के परिक्रमण से निरन्तर ऊर्जा का उत्सर्जन होता है तो रेखीय स्पेक्ट्रम के स्थान पर सतत स्पेक्ट्रम (continuous spectrum) प्राप्त होना चाहिए था। दूसरे शब्दों में, स्पेक्ट्रम में निश्चित आवृत्ति की रेखाएँ नहीं होनी चाहिए, परन्तु वास्तव में परमाणु का स्पेक्ट्रम सतत नहीं होता। इसके स्पेक्ट्रम में निश्चित आवृति’ की कई रेखाएँ होती हैं। अतः रदरफोर्ड परमाणु मॉडल परमाणुओं के रैखिक स्पेक्ट्रम (line spectrum) को समझाने में असफल रहा है।
रदरफोर्ड के परमाणु मॉडल की कमियों को दूर करने के लिए नील बोर ने सन् 1913 में स्पेक्ट्रमी अध्ययन और क्वाण्टम सिद्धान्त की सहायता से अपना परमाणु सिद्धान्त तथा परमाणु मॉडल प्रस्तुत किया।
प्रश्न 2.
बोर के परमाणु मॉडल का वर्णन कीजिए तथा उसकी सीमाएँ भी लिखिए।
उत्तर :
बोर का परमाणु मॉडल यह प्लांक के क्वाण्टम सिद्धान्त (Planck’s quantum theory) पर आधारित है। यह रदरफोर्ड के परमाणु मॉडल में पाये जाने वाले दोषों को दूर करता है और परमाणु के स्थायित्व व उसके रैखिक स्पेक्ट्रम की व्याख्या करता है। नील बोर (Neils Bohr, 1913) ने परमाणु संरचना के सम्बन्ध में निम्नलिखित अभिकल्पनाएँ (assumptions) प्रस्तुत की
1. इलेक्ट्रॉन नाभिक के चारों ओर किसी विशेष वृतीय कक्ष (circular orbit) में बिना ऊर्जा का | उत्सर्जन (emission) किये चक्कर लगाते रहते हैं। इन कक्षों को स्थायी कक्षाएँ (stationary orbits) कहते हैं।
2. नाभिक के चारों ओर अनेक वृत्तीय कक्षाएँ सम्भव हैं परन्तु इलेक्ट्रॉन इन सभी सम्भव कक्षाओं में चक्कर नहीं लगाते हैं। इलेक्ट्रॉन केवल उसी कक्षा में चक्कर लगाते हैं जिसमें उसका कोणीय संवेग का गुणित (integral multiple) होता है। यदि m द्रव्यमान का इलेक्ट्रॉन, r त्रिज्या वाली कक्षा में v वेग से घूमता है, तो इलेक्ट्रॉन का कोणीय संवेग
जहाँ, h प्लांक नियतांक है।
n स्थायी कक्षा की क्रम संख्या (principal quantum number) है। n= 1, 2, 3, … या K, L, M, N …
यदि किसी इलेक्ट्रॉन का कोणीय संवेग h/2π हैं, तो वह परमाणु के K-कोश में चक्कर लगाता है। इसी प्रकार यदि किसी इलेक्ट्रॉन का कोणीय संवेग अर्थात्
है, तो वह परमाणु के L-कोश (n=2) में चक्कर लगाती है।
3. प्रत्येक स्थायी कक्षा की एक निश्चित ऊर्जा होती है। इसलिए इन कक्षाओं को ऊर्जा स्तर (energy level) भी कहते हैं। जैसे-जैसे मुख्य क्वाण्टम संख्या (n) का मान बढ़ता है वैसे-वैसे स्थायी कक्षा की त्रिज्या (r) और उसकी ऊर्जा (E) का मान बढ़ता जाता है। जब तक इलेक्ट्रॉन एक-निश्चित ऊर्जा वाली स्थायी कक्षा में घूमता रहता है, तो वह ऊर्जा का शोषण या उत्सर्जन नहीं कर सकता।
4. जब कोई इलेक्ट्रॉन एक स्थायी कक्षा (ऊर्जा स्तर) से दूसरी स्थायी कक्षा (ऊर्जा स्तर) में कूदता है, तो दोनों ऊर्जा स्तरों की ऊर्जा का अन्तर (∆E) एक विकिरण के रूप में अवशोषित (absorb) या उत्सर्जित (emit) होता है। इस विकिरण की आवृत्ति (v) या तरंगदैर्घ्य (λ) का मान निम्नलिखित समीकरण से निकाल सकते हैं। जब इलेक्ट्रॉन एक न्यून ऊर्जा (E1) के स्तर से एक उच्च ऊर्जा (E2) के स्तर में कूदता है, तो परमाणु द्वारा ∆E ऊर्जा अवशोषित होती है। इसके विपरीत, यदि इलेक्ट्रॉन एक-उच्च ऊर्जा (E2) स्तर से एक न्यून ऊर्जा (E1) के स्तर में कूदता है तो ऊर्जा विकिरण के रूप में परमाणु द्वारा उत्सर्जित होती है।
5.इन परिवर्तनों के फलस्वरूप प्राप्त स्पेक्ट्रम में निश्चित आवृति की रेखायें (lines) उत्पन्न होती हैं। इस प्रकार यह मॉडल परमाणु के रैखिक स्पेक्ट्रम की व्याख्या करता है।परमाणु में इलेक्ट्रॉन हमेशा निम्नतम ऊर्जा वाली कक्षाओं में रहते हैं। इस अवस्था को परमाणु की आद्य अवस्था (ground state) कहते हैं। बाहर से ऊर्जा देने पर इलेक्ट्रॉन उत्तेजित (excite) होकर अधिक ऊर्जा वाली कक्षाओं में कूद जाते हैं। परमाणु की इस अवस्था को उत्तेजित अवस्था (excited state) कहते हैं। परमाणु को बाहर से बहुत अधिक ऊर्जा देने पर इलेक्ट्रान परमाणु को छोड़कर उससे बाहर निकल जाते हैं और धनायन (cation) प्राप्त होते हैं।
बोर के परमाणु मॉडल की सीमाएँ निम्नवत् हैं-
1.बोर का परमाणु मॉडल केवल उन परमाणुओं और आयनों के स्पेक्ट्रम की व्याख्या करता है। जिनमें केवल एक इलेक्ट्रॉन होता है; जैसे-H-परमाणु, He+ और Li2+ आयन। यह उन निकायों (systems) की व्याख्या नहीं करता जिनमें एक से अधिक इलेक्ट्रॉन होते हैं। जैसे-N, ,0, Cl आदि।
2. बोर के सिद्धान्त द्वारा जीमनं प्रभाव (Zeeman effect) और स्टार्क प्रभाव (Stark effect) की व्याख्या नहीं की जा सकती है। जिस वस्तु से विकिरण का उत्सर्जनं हो रहा है उस वस्तु को चुम्बकीय क्षेत्र में रखने पर उसकी स्पेक्ट्रम रेखाएँ विभक्त (split) हो जाती हैं। इस प्रकार स्पेक्ट्रम रेखाओं का चुम्बकीय क्षेत्र में विभक्त होना जीमन-प्रभाव (Zeeman effect) कहलाता है। इसी प्रकार वैद्युत क्षेत्र में स्पेक्ट्रम रेखाओं का विभक्त होना स्टार्क प्रभाव कहलाता है।
यह हाइड्रोजन परमाणु के सूक्ष्म स्पेक्ट्रम की संरचना (fine spectrum of H-atom) की व्याख्या नहीं करता है।
3. जब हाइड्रोजन के स्पेक्ट्रम का अध्ययन उच्च विभेदन क्षमता (high resolving power) वाले स्पेक्ट्रोस्कोप (spectroscope) से करते हैं तो यह पाया जाता है कि प्रत्येक एकल रेखा (single line) वास्तव में कई सूक्ष्म रेखाओं (fine lines) से मिलकर बनी हैं। हाइड्रोजन स्पेक्ट्रम में इन सूक्ष्म रेखाओं को हाइड्रोजन परमाणु का सूक्ष्म स्पेक्ट्रम (fine spectrum of H-atom) कहते हैं। बोर का परमाणु मॉडल इसकी व्याख्या नहीं कर सकता है।
4. बोर का परमाणु मॉडल हाइजेनबर्ग के अनिश्चितता सिद्धान्त (Heisenberg’s uncertainty principle) के विरूद्ध है।
प्रश्न 3.
क्वाण्टम संख्याएँ क्या हैं? ये कितने प्रकार की होती हैं? इनमें से प्रत्येक को संक्षेप में समझाइए।
उत्तर :
क्वाण्टम संख्याएँ-जिन संख्याओं का प्रयोग करके हम परमाणु में इलेक्ट्रॉनों की ऊर्जा तथा स्थिति (नाभिक से दूरी, कक्षक की आकृति, अभिविन्यास तथा चक्रण की दिशा) से सम्बन्धित समस्त जानकारी प्राप्त कर सकते हैं, उन्हें क्वाण्टम संख्याएँ कहते हैं। क्वाण्टम संख्याएँ निम्नलिखित चार प्रकार की होती हैं।
1. मुख्य क्वाण्टम संख्या—यह क्वाण्टम संख्या परमाणु के इलेक्ट्रॉन के मुख्य ऊर्जा स्तर अथवा
कोश (shell) को व्यक्त करती है। इसे n से प्रदर्शित करते हैं। यह क्वाण्टम संख्या, परमाणु के इलेक्ट्रॉनों की ऊर्जा तथा नाभिक से उसकी कोश की औसत दूरी प्रदर्शित करती है। इसका मान ‘0 के अतिरिक्त कोई पूर्णांक 1, 2, 3, 4 इत्यादि हो सकता है। मुख्य ऊर्जा स्तरों को क्रमशः नाभिक से आरम्भ करके K, L, M, N आदि अक्षरों से भी व्यक्त करते हैं। इन कोशों हेतु ॥ का मान क्रमशः 1, 2, 3, 4 आदि होता है। अर्थात् ॥=1 का अर्थ है न्यूनतम ऊर्जा स्तर अर्थात् K-कोश
n=2 का अर्थ है L-कोश
n= 3 का अर्थ है M-कोश
n= 4 का अर्थ है N-कोश इत्यादि।
n का मान बढ़ने के साथ-साथ इलेक्ट्रॉन की ऊर्जा तथा उसकी नाभिक से औसत दूरी प्राय: बढ़ती जाती है।
2. दिगंशी क्वाण्टम संख्या—इसे कोणीय संवेग (angular momentum) या भौम क्वाण्टम संख्या (secondary quantum number) भी कहते हैं। इसे 1 से प्रदर्शित करते हैं। तत्त्वों के स्पेक्ट्रमों में मुख्य रेखाओं के अतिरिक्त बारीक रेखाएँ भी होती हैं। इन बारीक रेखाओं की उत्पत्ति को समझाने के लिए यह सुझाया गया कि किसी बहुइलेक्ट्रॉनिक परमाणु के मुख्य कोश में उपस्थित इलेक्ट्रॉनों की ऊर्जा समान नहीं होती है। ऐसा इसलिए होता है क्योंकि ये इलेक्ट्रॉन विभिन्न पथों पर गति करते हैं और इनके कोणीय संवेग भी भिन्न-भिन्न होते हैं। अत: एक ही मुख्य कोश में अनेक उपकोश (sub-shell) अथवा ऊर्जा के उपस्तर (sub levels) होते हैं। इनके कारण ही इलेक्ट्रॉनों की कूदों (jumps) की संख्या बढ़ जाती है जिससे स्पेक्ट्रम में अधिक संख्या में रेखाएँ प्राप्त होती हैं।
दिगंशी क्वाण्टम संख्या 1, इलेक्ट्रॉन के उप ऊर्जा-स्तर (उपकोश) को प्रदर्शित करती है। के मान मुख्य क्वाण्टम संख्या n पर निर्भर करते हैं। किसी n के लिये । के मान 0 से लेकर (n-1) तक होते हैं।
n=1 तो, 1= 0
n=2 तो, 1=0 और 1
n=3 तो,1= 0, 1 और 2
जिन उपकोशों के लिये । के मान क्रमश: 0, 1, 2 और 3 होते हैं उन्हें क्रमशः s, p, d और f अक्षरों द्वारा प्रदर्शित करते हैं।
1 का मान उप ऊर्जा-स्तर का प्रतीक
किसी n के लिये 1 के मानों की कुल संख्या ॥ के बराबर होती है अर्थात् किसी कोश में उपकोशों की कुल संख्या उस कोश की मुख्य क्वाण्टम संख्या n के बराबर होती है।। का मान । उपकोश के कक्षकों की आकृति को निर्धारित करता है।
3. चुम्बकीय क्वाण्टम संख्या—इसे m या m; द्वारा प्रदर्शित करते हैं।
यह क्वाण्टम संख्या उप ऊर्जा-स्तरों के कक्षकों को प्रदर्शित करती है। m के मान दिगंशी क्वाण्टम संख्या के मान पर निर्भर करते हैं। किसी m के मान +1 से लेकर -1 तक (शून्य सहित) या -1 से +1 तक होते हैं।
यदि l= 0 तो, m=0
1= 1 तो, m= + 1, 0 -1
1= 2 तो, m= + 2, + 1, 0, -1 -2
1= 3 तो, m= +3, +2, + 1, 0,-1,- 2,-3
किसी 1 के लिए m के मानों की कुल संख्या (21+1) होती है, अर्थात् किसी उपकोश में कक्षकों की कुल संख्या (21+ 1) होती है।
(जहाँ । उपकोश की दिगंशी क्वाण्टम संख्या है)।
कभी-कभी + चिन्हों को बिना किसी विभेद के प्रयोग किया जाता है। बाह्य चुम्बकीय क्षेत्र की अनुपस्थिति में किसी उपकोश में उपस्थित सभी कक्षकों की ऊर्जाएँ । समान होती हैं। ऐसे कक्षकों को समभ्रंश कक्षक (degenerate orbital) कहते हैं। बाह्य चुम्बकीय क्षेत्र की उपस्थिति में किसी एक उपकोश में उपस्थित कक्षकों की ऊर्जाओं में थोड़ा अन्तर आ जाता है। किसी स्पेक्ट्रमी रेखा के कई रेखाओं में विभक्त होने का कारण भी यह ऊर्जाओं में अन्तर है।
4. चक्रण क्वाण्टम संख्या—इसे s या m, से प्रदर्शित करते हैं। इस संख्या की आवश्यकता इसलिए पड़ी क्योंकि परमाणु में इलेक्ट्रॉन न केवल नाभिक के चारों ओर घूमता है बल्कि अपने अक्ष पर घूर्णन (चक्रण) करता है। यह संख्या इलेक्ट्रॉन के चक्रण की दिशा को प्रदर्शित करती है। इलेक्ट्रॉन के चक्रण की दिशा दक्षिणावर्त (clockwise) या वामावर्त (anticlockwise) हो सकती है। m के किसी मान के लिए : के केवल दो मान होते हैं- या
इन या
या
इन दोनों मानों को विपरीत दिशाओं को दर्शाते हुए तीरों (क्रमश: ↑ और ↓) द्वारा प्रदर्शित करते हैं। प्रत्येक इलेक्ट्रॉन का उसके चक्रण के कारण कोणीय संवेग होता है जिसका परिमाण निम्न व्यंजक से प्राप्त होता है।
चक्रण कोणीय संवेगसंवेग जहाँ
इस क्वाण्टम संख्या से पदार्थों के चुम्बकीय गुणों के विषय में भी जानकारी मिलती है। घूमता हुआ इलेक्ट्रॉन छोटे चुम्बक के समान व्यवहार करता है। यदि किसी कक्षक में दो इलेक्ट्रॉन होते हैं तो वे एक-दूसरे के प्रभाव को निरस्त कर देते हैं। यदि किसी परमाणु के सभी कक्षक पूर्णतः भरे होते हैं तो सभी इलेक्ट्रॉन एक-दूसरे के चुम्बकीय प्रभाव को नष्ट कर देते हैं और पदार्थ प्रतिचुम्बकीय (diamagnetic) होता है। ऐसा पदार्थ बाह्य चुम्बकीय क्षेत्र द्वारा प्रतिकर्षित होता है। दूसरी ओर यदि पदार्थ में कुछ अर्द्ध-पूर्ण कक्षक होते हैं तो इसमें उपस्थित इलेक्ट्रॉन एक-दूसरे के चुम्बकीय प्रभाव को पूर्णतः नष्ट नहीं कर पाते। ऐसा पदार्थ अनुचुम्बकीय (paramagnetic) होता है। यह पदार्थ बाह्य चुम्बकीय क्षेत्र की तरफ आकर्षित होता हैं।
एनसीईआरटी सोलूशन्स क्लास 11 रसायन विज्ञान पीडीएफ
- 1. रसायन विज्ञान की कुछ मूल अवधारणाएं
- 3. तत्वों का वर्गीकरण तथा गुणधर्मो में आवर्तिता
- 4. रासायनिक आबंधन तथा आण्विक संरचना
- 5. द्रव्य की अवस्थाएं
- 6. ऊष्मागतिकी
- 7. साम्यावस्था
- 8. अपचयोपचय अभिक्रियाएँ
- 9. हाइड्रोजन
- 10. S - ब्लॉक के तत्व
- 11. P - ब्लॉक के तत्व
- 12. कार्बनिक रसायन - कुछ आधारभूत सिद्धांत तथा तकनीकें
- 13. हाइड्रोकार्बन
- 14. पर्यावरणीय रसायन